Канд. техн. наук, доц. МУЛ ЕВ Ю. В.
Белорусский ордена Трудового Красного Знамени политехнический институт
Докт. техн. наук СМИРНОВ С. Н.
Московский ордена Ленина и ордена Октябрьской Революции энергетический институт
Метанол и этанол являются добавками к моторному топливу. Контроль состояния их параметров — актуальный вопрос в технологии топ- ливопроизводства.
Безынерционный контроль параметров метанола и этанола может быть организован на основе измерения их диэлектрических проницаемостей.
Опубликованные данные по диэлектрической проницаемости метанола и этанола в жидком состоянии [1—3] получены для отдельных точек. Зависимости, описывающие эти результаты, отсутствуют.
Для теоретического описания диэлектрической проницаемости ε полярных веществ (метанол и этанол и др.) можно применить формулу Кирквуда [4]
(ε-1)(2ε+1)9ε= 4πNAρ3M (α+μ2g3kT), (1)
где NA — число Авогадро;
ρ — плотность;
М — молекулярная масса;
α — поляризуемость смещения;
k — постоянная Больцмана;
T — температура.
В (1) дипольный момент молекулы для расчетов принимается постоянным, а изменение его величины с температурой и давлением учитывается фактором корреляции g. Получить его значение при изменении плотности и температуры полярных веществ теоретическими расчетами невозможно [5].
В современной молекулярно-статистической теории [6, 7] диэлектрическую проницаемость связывают с параметром у, определяющим вклад ориентационной поляризации,
y=4/9πρNμ2MkT, (2)
Так, например, в [6] предложено
ε-1ε+2=y-3y2+… . (3)
Результаты расчета по (3) для метанола, как показано на рис. 1, меньше экспериментальных при малых у и значительно превышают εэкс
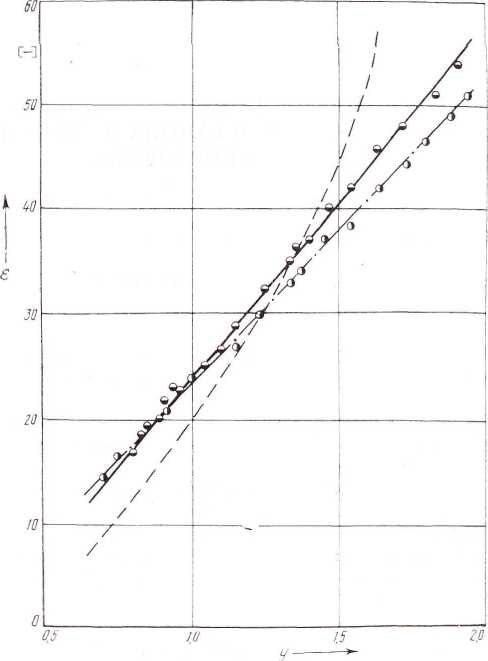
Рис. 1. Зависимость диэлектрической проницаемости метанола и этанола от параметра у:
——— - расчет ε метанола по (4); — — — — диэлектрическая проницаемость метанола по (3);
— · — — диэлектрическая проницаемость метанола по (6); ▄ — экспериментальные точки для метанола; ▐ — для этанола
при y> 1,7. Большие расхождения с опытными данными связаны со сложностью нахождения потенциала взаимодействия, который у полярных диэлектриков анизотропен. Для метанола и этанола, являющихся к тому же и ассоциированными веществами, определение даже энергии водородной связи представляет большую проблему [5].
Цель настоящей работы — создание методики, позволяющей рассчитывать диэлектрическую проницаемость метанола и этанола в жидком состоянии, на основе которой возможны интерполяция и экстраполяция с погрешностью, сопоставимой с точностью существующих экспериментальных данных.
Поставленная цель достигается анализом экспериментальных зависимостей диэлектрических проницаемостей метанола и этанола от параметра у. Для их построения взяты результаты измерения диэлектрической проницаемости метанола из [1]. Их диапазон составил: по давлению 0,1÷250 МПа, по температуре 223,1÷298,1 К (всего около 50 экспериментальных значений). Нами использованы значения диэлектрической проницаемости метанола из [3], где приведены 14 точек для температур от 298 до 513 К- Для принятых экспериментальных значений ε метанола, температурный интервал составил 20 К, по давлению — 50 МПа.
Для этанола экспериментальные данные по диэлектрической проницаемости наиболее полно представлены в [2]. Температурный диапазон составил 163÷333 К и по плотности — 0,74÷0,9 г/см3 (всего около 20 экспериментальных точек). В [3] описаны восемь значений ε этанола для температур 303÷513 К. Для метанола значения дипольных моментов приняты равными 1,68, для этанола 1,74D).
Значения диэлектрической проницаемости метанола и этанола [1—3] заимствованы только для представленных табличных величин. Для междушагового пространства в последующих расчетах они исключались. Значения плотности представлены в описанных источниках.
Таблица 1
Результаты аппроксимации зависимостей диэлектрических проницаемостей от параметра у для метанола и этанола

В результате расчетов зависимостей диэлектрических проницаемостей метанола и этанола от параметра у на основе массива из [1—3] построены зависимости (рис. 1). Очевидно, что нанесенные экспериментальные точки образуют в большей части линейные участки. Предельное значение параметра у, полученное в расчете, для рассмотренных веществ равно 2,02. Для этанола нижнее значение параметра у — 0,8. Для меньших его значений экспериментальные данные отсутствуют. Для метанола при y<0,6 наблюдается отклонение точек от линейной зависимости. Это свидетельствует о существовании при таких значениях у паровой фазы.
Таблица 2
Диэлектрическая проницаемость метанола εм и этанола εэ при плоскостях 0,6 и 0,65 г/см3
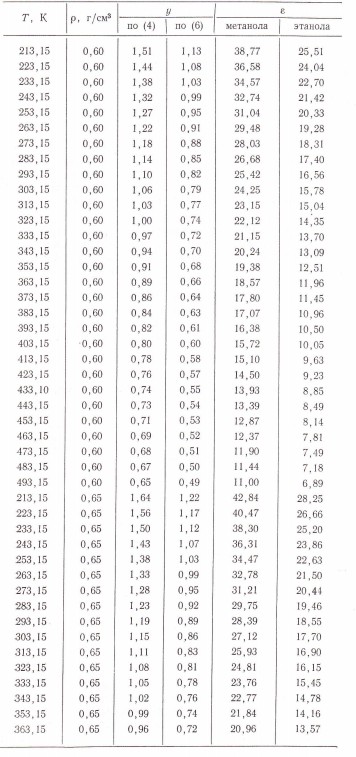
Продолжение таблицы 2
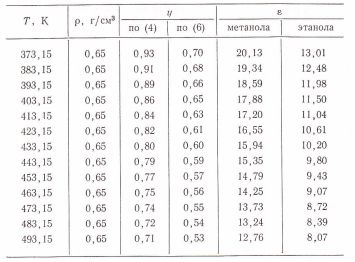
Если для этанола все экспериментальные точки расположены на прямой, то для метанола выделяются три точки (рис. 1), которые явно отклонены от линейного вида, не имеют связи ни с температурой, ни с плотностью и их можно отнести к промахам.
Полученные зависимости аппроксимированы прямой линией. Для рассмотренных веществ ее параметры определены методом наименьших квадратов [8]. Расчеты проведены для у с учетом и без учета составляющей поляризации смещения. В результате получены уравнения, показанные в табл. 1.
Из табл. 1 видно, что лучшее совпадение с экспериментом (наименьшие среднеарифметические и среднеквадратичные отклонения) для значений у метанола и этанола имеют уравнения (5) и (7), т. е. учет составляющей поляризации смещения приводит к уменьшению отклонения экспериментальных точек от линейности.
Практическое использование полученных уравнений (5) и (7) проиллюстрировано интерполяцией при плотностях 0,6 и 0,65 г/см3 (табл. 2) и экстраполяцией в неисследованные области параметров (табл.3).
ВЫВОДЫ
1. Современная молекулярно-статистическая теория диэлектриков не позволяет описать зависимость ε=f(y) метанола и этанола в широком диапазоне параметров.
2. Предложенная методика дает возможность проводить расчет диэлектрической проницаемости метанола и этанола закритических плотностей в пределах у до 2,02 с погрешностью, сопоставимой с точностью существующих экспериментальных данных.
Таблица 3
Диэлектрическая проницаемость метанола и этанола при плоскостях 0,9 и 1,0 г/см3
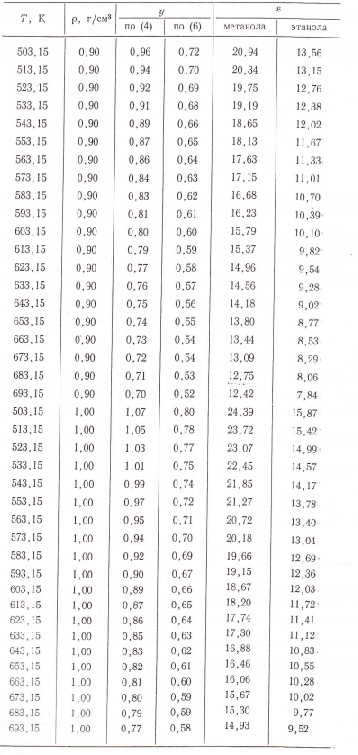
ЛИТЕРАТУРА
1. Ledwig R., Wurflinger А. Dielectric Measurements at High Pressures and Low Temperatures Dielectric and pVT Data of Metanol//Zeitschrift for Physikalische Chemie, 1982,—Bd 132,—S. 21—27.
2. Timmermans J. The phys-chemist constants of binary Systems in concentrated solvente J. Phys. Chem.—1959.— V. 2.—• P. 1272.
3. Dannhauser W., В a h e L. W. Dielectric Constant of Hydrogen Bonded liquids. 3. Superbead alcohols//J. Chem. Phys.—1964.— V. 40.— N 10.— P. 3058—3066.
4. Kirkwood J. G. On the theory of dielectric polarization // J. Chem. Phys.— 1936,—V. 4,—N 3,—P. 592—601.
5. Смирнов С. H. Расчетно-экспериментальное определение диэлектрической проницаемости сжатых газов, газовых смесей и таблицы для автоматизации контроля теплофизических свойств: Дис. ... докт. техн. наук.— М.: МЭИ, 1986.—600 с.
6. Р a t е у G. N. An integral equation theory for the dence dipolar hard-sphere fluid // Mol. Phys.—1977,—V. 34,—N 2,— P. 427—440.
7. Adams D. J. Computer simulation of highly polar liguids: the hard spheres plus point dipole potential // Mol. Phys.'—1980.— V. 40,-—N 5.— P. 1261—1271.
8. Гусак А. А. Элементы методов вычислений.— Мн.: Изд-во БГУ, 1982.—166 с.
Представлена НТС кафедры ВТ и СУ Поступила 6.05.1991